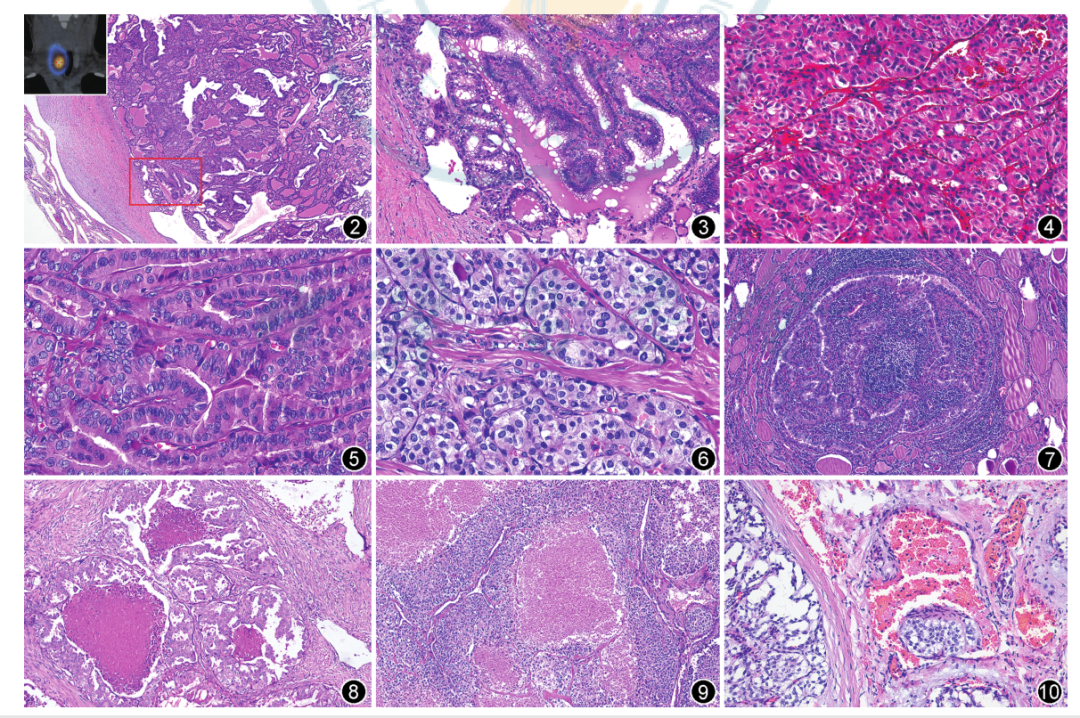
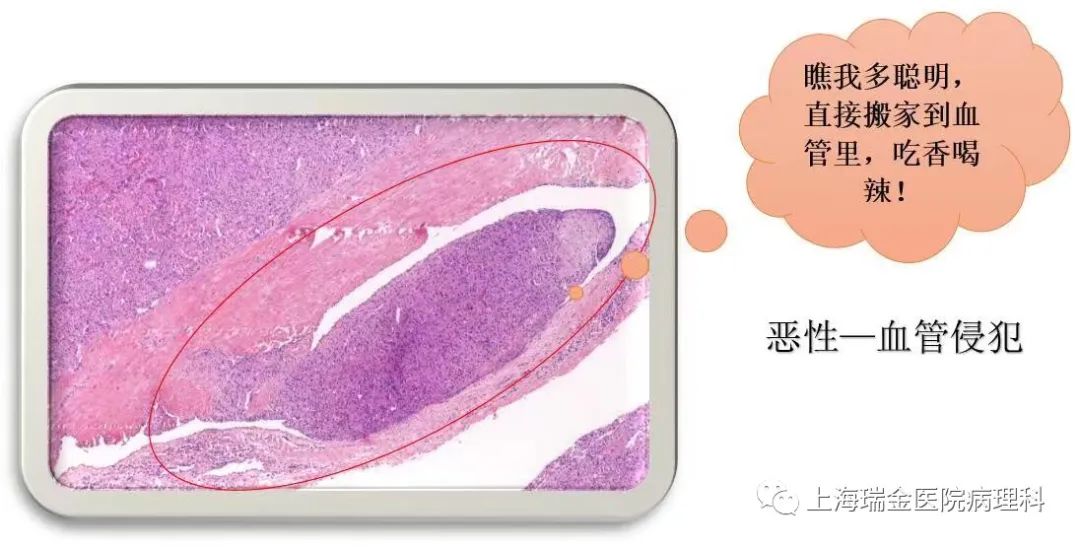
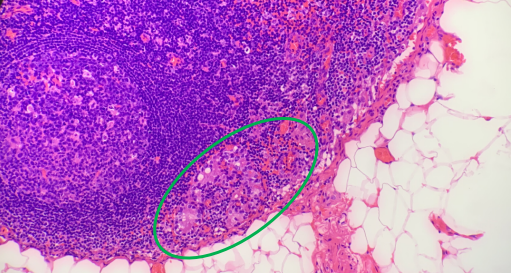
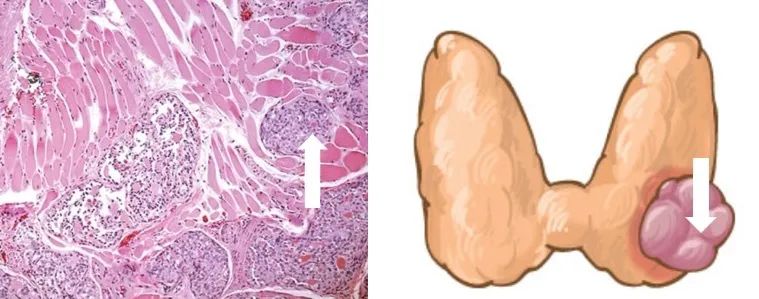
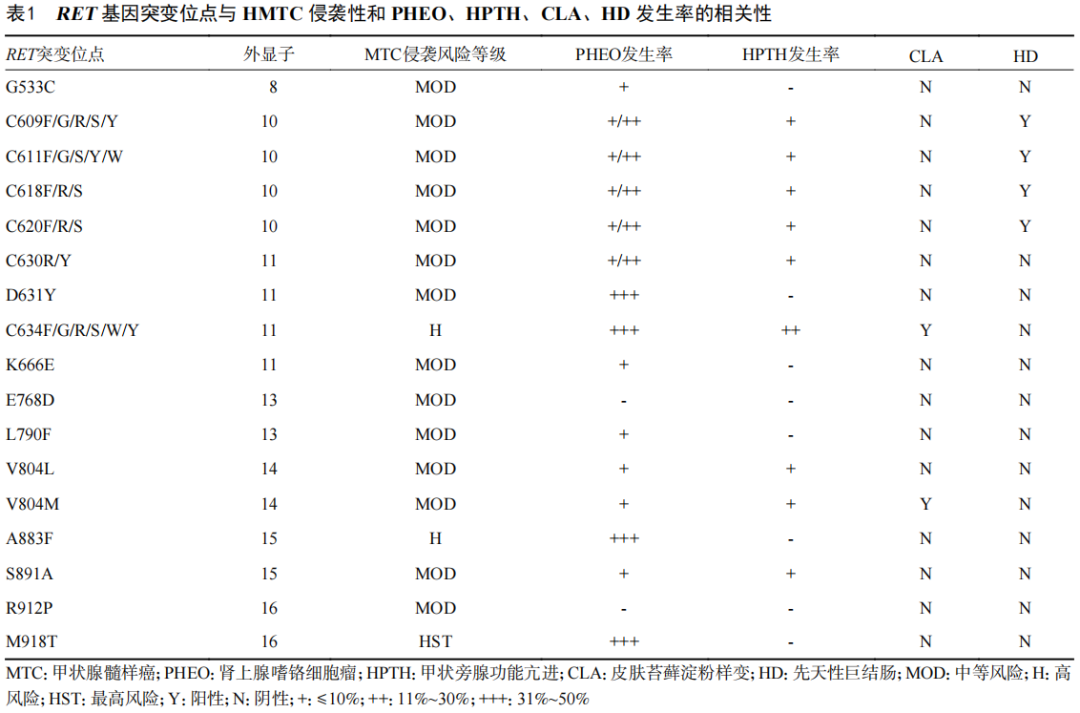
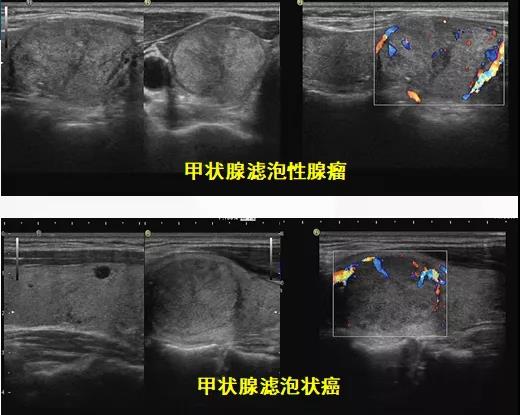
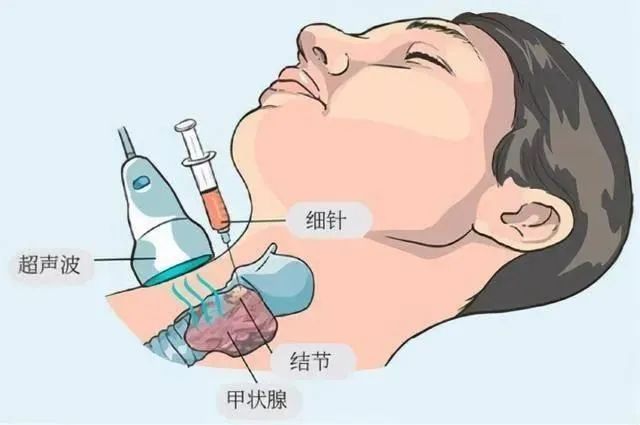
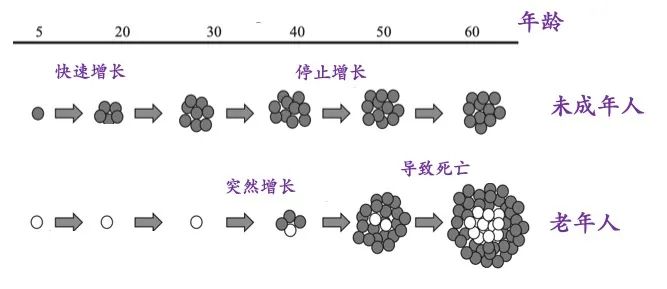
摘 要 第5版WHO甲状腺肿瘤分类以细胞发生机制为新分类框架的基础,以组织学、分子和临床生物学特征来判定肿瘤分类和亚型。甲状腺滤泡起源的肿瘤为甲状腺内最常见的肿瘤,包括良性、低风险和恶性肿瘤。良性肿瘤包括滤泡腺瘤、常伴有甲状腺功能亢进的乳头状滤泡腺瘤、嗜酸性细胞腺瘤和新概念甲状腺滤泡结节性病变。低风险肿瘤包括具有乳头样核特征的非浸润性甲状腺滤泡性肿瘤、恶性潜能未定的肿瘤和透明变梁状肿瘤。滤泡起源的恶性肿瘤根据分子特征和侵袭性分为BRAF样恶性肿瘤和RAS样恶性肿瘤。不提倡≤1 cm的乳头状癌作为独立亚型,而应根据形态特征进行亚分型。提出高级别甲状腺滤泡细胞起源癌,包括传统低分化癌、高级别分化型甲状腺癌,形态特征为核分裂象增加、肿瘤坏死、不伴有间变特征,临床生物学行为相似。鳞状细胞癌为间变性癌的一种亚型。 正 文 2022年第5版WHO对甲状腺肿瘤的定义、分类、组织学分级、分子分型等方面做了修订,对病理诊断和临床实践工作均会产生系列影响,需要临床及病理医师尽快了解。甲状腺肿瘤总体可分为上皮性肿瘤、非上皮性肿瘤和继发肿瘤三大类,其中后两者与其他器官分类一致,本文对甲状腺滤泡上皮细胞起源的肿瘤分类及其分子特征进行解读。 第5版WHO甲状腺肿瘤分类结合肿瘤形态特征、突变和转录组学特征,提出RAS样和BARF样肿瘤。RAS样分子异常包括BRAF K601E、DICER1、EZH1、EIF1AX突变和PPARG、THADA融合;BARF V600E样分子异常包括ALK、BRAF、RET、NTRK1/3和MET融合。RAS样肿瘤通常有包膜或界限清楚、肿瘤以滤泡结构为主,多数表现为RAS样基因异常而缺乏BRAF突变;其肿瘤细胞甲状腺乳头状癌(papillary thyroid carcinoma,PTC)核特征不明显,核内假包涵体罕见,称为RAS样核。BRAF样肿瘤通常具有乳头状结构、典型PTC细胞核特征;多数为浸润性,但也可呈膨胀性生长或为囊性。其肿瘤细胞核重叠,毛玻璃样,可见核沟、核内假包涵体,称为BRAF样核。但这种形态学评估无疑存在判读差异。 一、肿瘤分类 甲状腺滤泡上皮细胞起源的肿瘤可分为良性、低风险和恶性肿瘤。PTC细胞核特征、浸润、高级别形态学特征,如坏死、核分裂象、间变性癌形态特征等在甲状腺滤泡源性肿瘤分类中起关键作用(图1)。 (一)良性肿瘤 良性肿瘤包括甲状腺滤泡腺瘤(follicular thyroid adenoma)、嗜酸细胞腺瘤(oncocytic adenoma of the thyroid)、新增的甲状腺滤泡结节性病变(thyroid follicular nodular disease)、具有乳头状结构的滤泡腺瘤(follicular adenoma with papillary architecture)4种。 1. 滤泡结节性病变:通常有部分多结节性甲状腺肿伴腺瘤样增生/腺瘤样结节为克隆性病变、为腺瘤,而另一部分则为增生。甲状腺激素通路相关基因异常发挥重要作用,如甲状腺球蛋白(Tg)、甲状腺过氧化物酶(TPO)、钠碘转运蛋白、双氧化酶、XB130、TSHR等,是最常见的甲状腺滤泡结节性病变致病基因。家族性和早发性甲状腺滤泡结节性病变可能与DICER1综合征相关。 2. 滤泡腺瘤和嗜酸细胞腺瘤:滤泡腺瘤为克隆性肿瘤性增生。第5版WHO强调其超声表现为实性、边界清楚的均质强回声或等回声冷结节,以区别于具有乳头状结构的滤泡腺瘤。含75%以上嗜酸性肿瘤细胞的滤泡性肿瘤为嗜酸细胞肿瘤,其中良性者为嗜酸细胞腺瘤。 3. 乳头状甲状腺滤泡腺瘤:具有特征性滤泡内“向心性”乳头的滤泡腺瘤(图2,3),细胞核圆而一致,缺乏PTC细胞核特征。临床上具有甲状腺功能亢进或亚临床甲亢,核素扫描表现为“高功能性热结节”(图2角图)。手术切除肿瘤后甲状腺功能可恢复正常。这些肿瘤通常与TSHR突变激活(高达70%)或GNAS突变(少部分)和/或EZH1突变有关。是McCune-Albright综合征以及Carney综合征的特征之一,前者由胚系嵌合体GNAS突变所引起,后者由PRKAR1A中的胚系失活突变引起。 图2~10 图2示乳头状甲状腺滤泡腺瘤,图2角图为核素扫描,显示肿瘤为“高功能性热结节” 图3为图2中红色矩形图内放大图像 图4 嗜酸细胞肿瘤,肿瘤细胞均具有嗜酸性胞质,不具有PTC细胞核特征 图5 高细胞型甲状腺乳头状癌 图6 实体型甲状腺乳头状癌 图7 Warthin样型甲状腺乳头状癌 图8 高级别滤泡上皮细胞起源的癌、高级别分化型甲状腺癌 图9 甲状腺低分化癌 图10 伴RET-NCOA4基因融合的甲状腺乳头状癌,图中央可见血管内癌栓 (二)低风险肿瘤 低风险肿瘤具有极低转移可能,是指在形态和临床特征上介于良性和恶性肿瘤之间的交界性肿瘤,组织学分类包括具有乳头状核特征的非浸润性甲状腺滤泡性肿瘤(non-invasive follicular thyroid neoplasm with papillary-like nuclear features,NIFTP)、恶性潜能未定的甲状腺肿瘤(thyroid tumors of uncertain malignant potential)、透明变梁状肿瘤(hyalinizing trabecular tumour)。 1. NIFTP:它的诊断在延续第4版WHO中组织学诊断标准的基础上,强调需除外BRAF V600E、TERT启动子、TP53/ target=_blank class=infotextkey>P53基因等高危突变。此外,新增了直径2 mm~1 cm的NIFTP和嗜酸细胞型NIFTP(至少含75%的嗜酸细胞构成)。NIFTP细胞核特征判读具有不同差异,亚洲国家NIFTP发生率(0.3%~5.0%)远低于西方国家(15%~20%),为极度惰性肿瘤,单纯肿瘤完全切除和单腺叶切除的治疗方案已可治愈,如无可疑临床特征,可视作滤泡腺瘤进行随访。 2. 恶性潜能未定的甲状腺肿瘤:为有或无包膜但边界清楚,在彻底取材和详尽检查后,可疑包膜和/或脉管、周围正常组织浸润的甲状腺肿瘤。根据是否具有PTC核特征可分为恶性潜能未定的滤泡性肿瘤(不具有PTC细胞核特征)、恶性潜能未定的高分化肿瘤(具有不同程度PTC细胞核特征)。滤泡腺瘤、NIFTP、恶性潜能未定的甲状腺肿瘤、滤泡癌、浸润性包裹性滤泡亚型PTC的鉴别诊断标准为对细胞核特征和包膜/血管侵犯的主观评估(图1),同样具有明显观察者差异。 3. 透明变梁状肿瘤:其病理诊断标准、免疫表型均无明显更新。但强调透明变梁状肿瘤缺乏BRAF和RAS突变,PAX8-GLIS1/GLIS3基因重排为透明变梁状肿瘤关键分子特征。单纯甲状腺叶切除术通常可治愈。有过极少数发生淋巴结或远处转移的报道。恶性透明变梁状肿瘤有肿瘤包膜或血管浸润。 甲状腺叶切除术结合临床和影像学监测是治疗NIFTP和透明变梁状肿瘤的首选方法。术后应避免放射性碘治疗,因为几乎都呈良性病程。因其恶性潜能未定需密切随访。 (三)恶性肿瘤 恶性肿瘤包括分化型甲状腺癌(differentiated thyroid carcinoma,DTC)、高级别分化型甲状腺癌(differentiated high grade thyroid carcinoma,DHGTC)、低分化甲状腺癌(poorly differentiated thyroid carcinoma,PDTC)和间变性癌(anaplastic thyroid carcinoma)。DTC不伴有高级别形态特征,包括:PTC、甲状腺滤泡癌(follicular thyroid carcinoma,FTC)、嗜酸细胞癌(oncocytic carcinoma of the thyroid)中不伴有高级别组织学特征者(图4)。 1. PTC:它是成人和儿童中最常见的滤泡细胞起源的恶性肿瘤,通常为散发性。少数≤1.0 cm PTC表现出侵袭性病理特征和临床行为,临床管理指南制定PTC患者个性化风险分层方案依赖于多种病理特征,而非单纯依靠肿瘤大小,因此第5版WHO不推荐将“微小乳头状癌”视为独立PTC亚型。经典型PTC定义为由具有典型PTC细胞核特征的肿瘤细胞形成典型乳头。淋巴管浸润是PTC区域淋巴结转移率高的原因,血管侵犯少见。包裹性亚型包膜完整、部分或全层被肿瘤浸润。非浸润性包裹性经典型PTC预后良好。在PTC亚型中,高细胞(tall cell;图5)、柱状细胞(columnar cell)和鞋钉(hobnail)型具有侵袭性临床特征,具有中度复发风险。弥漫硬化型(diffuse sclerosing)PTC的特点是甲状腺弥漫性单侧或双侧受累,广泛淋巴管浸润,致密硬化,大量沙砾体和慢性淋巴细胞性甲状腺炎。实性/梁状亚型具有实性、梁状或巢状的生长模式(图6),但缺乏坏死和明显的核分裂象。弥漫硬化型和实性亚型PTC也可能为侵袭性临床病程。其他预后未知的亚型包括:嗜酸、Warthin样(图7)、透明细胞亚型。梭形细胞PTC和伴有纤维瘤病/筋膜炎样/硬纤维样间质的PTC少见。前者可能难以诊断,后者是一种罕见的肿瘤,有2种不同的成分:PTC和伴有CTNNB1基因突变/β-catenin异常表达细胞核的纤维瘤病间质。第5版WHO强调滤泡亚型PTC有2种不同的亚型,包括浸润性滤泡亚型PTC以及包裹性滤泡亚型PTC。前者缺乏包膜,除乳头状结构外,具有典型PTC的所有特征,常表现为神经周围和淋巴管浸润,通常为BRAF样肿瘤。相反,包裹型类似于FTC,呈境界清晰的膨胀性生长,伴或不伴有刺激纤维反应形成的肿瘤包膜;随后会侵犯局部包膜或毗邻组织(如无包膜),当出现脉管侵犯时,受累的通常是肿瘤包膜和/或血管而非淋巴管,通常为RAS样肿瘤。在第5版WHO中筛状-桑葚型甲状腺癌(cribriform morular thyroid carcinoma)不再为PTC亚型,而为组织来源未定的肿瘤。该肿瘤几乎均表现为Wnt信号通路的基因改变(APC基因突变最常见),而无BRAF V600E突变,肿瘤细胞免疫表型β-catenin异常表达于细胞质和细胞核、阳性表达雌激素和孕激素,通常缺乏PAX8和甲状腺球蛋白的表达。 2. FTC、嗜酸细胞癌与浸润性包裹性滤泡亚型PTC(invasive encapsulated follicular variant papillary carcinoma):FTC定义为甲状腺滤泡上皮细胞起源、缺乏PTC细胞核特征的恶性肿瘤,大约占甲状腺癌10%,5年生存率近88%,10年生存率为78%。通常具有包膜,浸润性生长。鉴别诊断上FTC和滤泡腺瘤的组织学特征为包膜和/或血管浸润;与浸润性包裹性滤泡亚型PTC之间的鉴别点在于缺乏PTC细胞核特征。第5版WHO甲状腺肿瘤分类指出,在诊断嗜酸细胞癌时,除了浸润程度外,需评估核分裂象(每2 mm2≥3个)和肿瘤坏死,以判定肿瘤是否进展为嗜酸性PDTC。嗜酸细胞癌可转移到淋巴结,嗜酸细胞癌通常经血道播散至远处,远处转移的比例为15%~27%,在伴有广泛血管浸润的病例中高达40%。 嗜酸细胞癌的预后参数包括患者年龄、肿瘤大小、血管侵犯、甲状腺外侵犯和是否存在远处转移。5年总生存率为85%,但在诊断时有远处转移的患者仅有24%,而无远处转移的患者这一比例为91%。由于放射性碘治疗嗜酸细胞癌的效果比FTC差,一旦疾病复发,治疗更加困难。 浸润性包裹性滤泡亚型PTC诊断标准参考FTC包膜和/或血管浸润的判定标准,临床生物学行为与FTC相似。浸润性包裹性滤泡亚型PTC、FTC和嗜酸细胞癌根据浸润、细胞核特征和/或程度进一步分为:(1)微小浸润型(仅包膜浸润);(2)包裹性血管浸润型(有血管浸润、有或无包膜浸润);(3)弥漫浸润型。该分类在动态风险分层和临床处理中至关重要。微小浸润型FTC 40个月无病存活率为97%,为低风险,单纯局部切除即可治愈;血管浸润型FTC为81%;广泛浸润型FTC为45%,需要行甲状腺全切术和辅助治疗,以防止局部复发和/或远处转移。 3. 高级别滤泡细胞起源的癌(follicular-derived carcinomas,high-grade):首先需除外间变性癌形态学特征,具有高级别形态学特征之一(高核分裂活性、肿瘤坏死),中等预后风险。高级别滤泡细胞起源的癌:(1)Turin分类中的PDTC;(2)高级别分化型甲状腺癌(DHGTC,图8):具有高分化癌的相应组织结构和/或细胞学特性,如PTC核特征和/或结构、FTC的滤泡生长模式。两者组织学异同为:(1)PDTC呈实性、小梁状或岛状生长(图9);DHGTC绝大多数呈乳头状。(2)“葡萄干样”核:少数PDTC肿瘤细胞有;DHGTC则无。(3)肿瘤坏死:两者均可有。(4)PDTC核分裂计数≥3/2 mm2,而DHGTC为≥5/2 mm2。(5)PTC细胞核特征:PDTC中无;DHGTC中可有或无。(6)DHGTC常见血管、淋巴管、神经周围浸润和甲状腺外侵犯。两者均不同程度表达滤泡上皮细胞免疫标志物,Ki-67阳性指数高,通常在10%~30%之间。高级别滤泡细胞起源的癌十分罕见,占比低于1.0%~6.7%。欧洲和南美洲国家的患病率较高,在北美国家和日本则相反。多发生于50岁以上成年人,进展迅速,女性占比略高。3%~50%的病例伴有淋巴结转移。大约50%的高级别滤泡细胞起源的癌不摄取放射性碘。PDTC 10年总存活率为46%,疾病特异生存率为60%,高级别滤泡细胞起源的癌大致与其相似。与PDTC相比,高级别PTC的无病存活率可能更差。嗜酸性与非嗜酸性PDTC的预后相似。青少年PDTC罕见,多数存在DICER1的体系或胚系突变,肿瘤病死率为30%。 4. 甲状腺间变性癌:甲状腺鳞状细胞癌因具有类似间变性癌的免疫表型和分子表型,第5版WHO中更新为间变性癌的一种组织学类型。此外,强调必须对所有间变性癌进行快速、及时的BRAF V600E突变检测,因BRAF和MEK联合抑制剂对BRAF V600E突变型间变性癌有效。 二、分子特征 分化型甲状腺癌通常由MAPK信号通路和AKT信号通路调节基因的极少数体细胞突变或融合引起(图10),其形态学特征主要与RAS和BRAF突变有关,两者为癌变过程中的早期驱动事件(图11)。PDTC和DHGTC通常由分化型甲状腺癌以遗传多步骤的方式进展而来,表现为BRAF、RAS或少数基因融合(常为RET或NTRK3)等早期驱动基因变异之外,再携带继发侵袭性突变,最常见的是TERT启动子、少数PIK3CA和TP53等后期分子事件。青少年PDTC患者DICER1突变常见,可能反映了高级别特征和潜在miRNA调节障碍之间的耦合。 图11 AKT和MAPK信号通路参与甲状腺滤泡上皮细胞癌变示意图 与FTC或浸润性包裹性滤泡亚型PTC相比,PTC是“分化相对较差”的癌,其常见分子事件为点突变或基因重排。BRAF V600E突变在高细胞型PTC中最常见(约占90%)。柱状细胞型PTC与BRAF V600E突变有关,而BRAF融合、RAS突变、TERT启动子突变、CDKN2A缺失和TP53突变较为少见。大多数鞋钉型PTC存在BRAF V600E突变,通常与TP53、TERT启动子和PIK3CA突变相关。这些突变激活MAPK信号通路导致增殖、血管生成和侵袭性增强,并下调分化相关基因的转录。 因此具有包膜或界限清晰的滤泡结构的甲状腺肿瘤RAS样突变高发而BRAF V600E样突变少见。若在形态学良性或低风险甲状腺肿瘤中检测到BRAF V600E和高危突变,如TP53、PIK3CA或TERT启动子突变,则应仔细检查整个肿瘤以排除恶性。 PTC可发生多种癌症相关基因融合,其中RET、NTRK、BRAF和ALK均为临床治疗重要特定药物靶点。甲状腺癌相关RET重排和辐射诱导PTC密切相关,其融合伴侣基因中CCDC6最常见,其次是NCOA4。NTRK融合相对少见,3%~5%的BRAF野生型PTC患者,尤其是儿童和青少年中可查见NTRK融合。与BRAF突变病例相比,这些肿瘤以滤泡结构为主,通常表现为推挤性边界、透明细胞质、核异型性不明显。 此外,PTC还存在PLEKHS1基因异常,包括启动子突变、启动子异常甲基化和基因过表达导致AKT信号通路激活和预后不良。TERT、PLEKHS1启动子和/或TP53基因突变中的任一突变与BRAF或RAS突变协同均预示高分化甲状腺癌临床预后差。TERT启动子突变主要见于老年人,肿瘤体积较大,通常表现为广泛浸润;与放射性碘难治性疾病、远处转移和肿瘤去分化高度相关。此外,染色体5p15.33上TERT基因位点获得、TERT启动子甲基化异常和TERT mRNA过表达也预示高分化甲状腺癌预后不良。 9q和11q的丢失与癌症特异性病死率有关。过量染色体1q扩增以及mRNA处理器MED12和RBM10的突变,编码RNA聚合酶Ⅱ驱动转录和mRNA剪接功能的调节蛋白,这些基因突变见于PDTC和PTC亚型。表观遗传学异常与分化型甲状腺癌远处转移的风险增加有关。miR-146a/b、miR-221和miR-222等miRNA过表达与PTC不良预后有关。 嗜酸细胞肿瘤有特征性线粒体基因组(mtDNA)或GRIM19(NDUFA13)基因改变,三分之一以上有拷贝数异常,在电子传递链复合体Ⅰ亚单位基因中都存在同质或高度异质性(>70%)线粒体DNA突变。拷贝数变异引发近全基因组的单倍体化,伴或不伴有后续的基因组内复制。染色体改变与浸润程度有关:大多数仅有包膜浸润或局灶性血管浸润的嗜酸细胞癌证实是二倍体;而有广泛血管浸润和广泛侵袭性的肿瘤通常是多倍体,多有第7号染色体的扩增。此外,嗜酸细胞癌还存在复发性突变,包括RAS突变(突变率低于FTC)、EIF1AX、TERT、TP53、NF1、CDKN1A等。 从PTC或DHGTC发展而来的间变性癌通常携带TERT启动子突变和BRAF复合突变,而来自FTC或EFVPTC的间变性癌通常携带RAS和TERT启动子复合突变。此外常报道的有TP53基因突变和CDKN2A/B基因缺失。与非错配修复基因突变病例相比,具有非错配修复基因突变的间变性癌表现为超突变表型,但其临床相关性尚不清楚。